為規(guī)范境內(nèi)第三類和進(jìn)口醫(yī)療器械注冊(cè)相關(guān)工作���,按照《醫(yī)療器械監(jiān)督管理?xiàng)l例》(國(guó)務(wù)院令第650號(hào))和《醫(yī)療器械注冊(cè)管理辦法》(食品藥品監(jiān)管總局令第4號(hào))要求�����,食品藥品監(jiān)管總局組織制修訂了自行撤回醫(yī)療器械注冊(cè)申請(qǐng)程序(自2016年1月1日起施行)���。
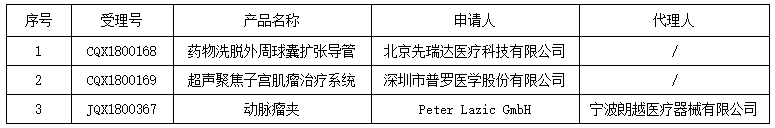
2019年7月16日,國(guó)家藥品監(jiān)督管理總局發(fā)布自行撤回醫(yī)療器械注冊(cè)申請(qǐng)告知書發(fā)布的通知��,共涉及3個(gè)產(chǎn)品��。詳情如下:
以下是自行撤回醫(yī)療器械注冊(cè)申請(qǐng)程序:
一����、項(xiàng)目名稱:自行撤回醫(yī)療器械注冊(cè)申請(qǐng)
二、受理范圍:已受理尚未做出行政許可決定前的注冊(cè)申請(qǐng)���。
三��、收費(fèi)依據(jù):不收費(fèi)
四�����、辦理?xiàng)l件:
由注冊(cè)人提出申請(qǐng)�����。
五�����、申請(qǐng)資料要求:
(一)注冊(cè)申請(qǐng)人簽章的自行撤回申請(qǐng)�,申請(qǐng)內(nèi)容應(yīng)當(dāng)清晰、完整�����;
(二)撤回注冊(cè)申請(qǐng)項(xiàng)目的受理通知書原件���。
(三)具體辦理人應(yīng)提交授權(quán)書及該身份證復(fù)印件����。
六�、辦理程序:
(一)行政事項(xiàng)受理服務(wù)和投訴舉報(bào)中心經(jīng)辦人按照相應(yīng)申請(qǐng)資料要求,對(duì)自行撤回注冊(cè)申請(qǐng)資料進(jìn)行形式審查��,對(duì)于符合申請(qǐng)資料要求的予以受理��。
(二)行政事項(xiàng)受理服務(wù)和投訴舉報(bào)中心自受理后3個(gè)工作日內(nèi)�����,按照申請(qǐng)事項(xiàng)實(shí)際審評(píng)審批狀態(tài)和有關(guān)移交程序規(guī)定,將申請(qǐng)資料移交總局醫(yī)療器械技術(shù)審評(píng)中心和總局醫(yī)療器械注冊(cè)管理司���。
(三)總局醫(yī)療器械技術(shù)審評(píng)中心或總局醫(yī)療器械注冊(cè)管理司核實(shí)后終止相關(guān)注冊(cè)資料審評(píng)審批���,并在電子審評(píng)記錄上予以標(biāo)注?���?偩轴t(yī)療器械注冊(cè)管理司應(yīng)告知總局醫(yī)療器械技術(shù)審評(píng)中心����。企業(yè)已交納的注冊(cè)費(fèi)用不予退回。
(四)總局醫(yī)療器械技術(shù)審評(píng)中心復(fù)印醫(yī)療器械注冊(cè)申報(bào)資料�����,將復(fù)印件歸檔�����,原件退還注冊(cè)申請(qǐng)人���。