2023年9月11日�,上海市藥品監(jiān)督管理局發(fā)布2022年度上海市有源醫(yī)療器械注冊(cè)現(xiàn)場(chǎng)核查常見問(wèn)題匯總數(shù)據(jù),2022年度上海市器審中心依據(jù)《醫(yī)療器械生產(chǎn)質(zhì)量管理規(guī)范》對(duì)有源類醫(yī)療器械生產(chǎn)企業(yè)(設(shè)備類���,不含獨(dú)立軟件產(chǎn)品)開展了127家次現(xiàn)場(chǎng)體系核查����,涉及核查產(chǎn)品為185個(gè),合計(jì)發(fā)現(xiàn)缺陷835項(xiàng)��,其中關(guān)鍵不符合項(xiàng)254項(xiàng)�����,一般不符合項(xiàng)581項(xiàng)���。
2023年9月11日,上海市藥品監(jiān)督管理局發(fā)布2022年度上海市有源醫(yī)療器械注冊(cè)現(xiàn)場(chǎng)核查常見問(wèn)題匯總數(shù)據(jù)�,2022年度上海市器審中心依據(jù)《醫(yī)療器械生產(chǎn)質(zhì)量管理規(guī)范》對(duì)有源類醫(yī)療器械生產(chǎn)企業(yè)(設(shè)備類,不含獨(dú)立軟件產(chǎn)品)開展了127家次現(xiàn)場(chǎng)體系核查���,涉及核查產(chǎn)品為185個(gè)���,合計(jì)發(fā)現(xiàn)缺陷835項(xiàng),其中關(guān)鍵不符合項(xiàng)254項(xiàng)����,一般不符合項(xiàng)581項(xiàng)��。
一��、上海市有源醫(yī)療器械注冊(cè)現(xiàn)場(chǎng)核查常見問(wèn)題總體情況
通過(guò)分析現(xiàn)場(chǎng)核查不符合項(xiàng)發(fā)現(xiàn)�����,127家次現(xiàn)場(chǎng)體系核查合計(jì)發(fā)現(xiàn)缺陷835項(xiàng)�,其中關(guān)鍵不符合項(xiàng)254項(xiàng)��,一般不符合項(xiàng)581項(xiàng)�。
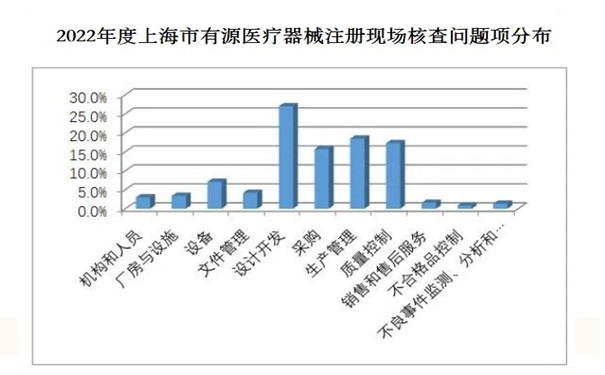
從不符合項(xiàng)在《規(guī)范》中各章節(jié)的分布情況來(lái)看,規(guī)范的11個(gè)章節(jié)均有涉及��。從各章節(jié)不符合項(xiàng)總數(shù)占比來(lái)看�,占據(jù)前四位的分別為設(shè)計(jì)開發(fā)(27%)、生產(chǎn)管理(18.5%)���、質(zhì)量管理(17.3%)和采購(gòu)(15.7%)��。不符合項(xiàng)分布情況詳見圖1��。
圖1.2022年度上海市有源醫(yī)療器械注冊(cè)現(xiàn)場(chǎng)核查問(wèn)題項(xiàng)分布
二�����、上海市有源醫(yī)療器械注冊(cè)現(xiàn)場(chǎng)核查常見問(wèn)題
從2022年度有源醫(yī)療器械的現(xiàn)場(chǎng)核查發(fā)現(xiàn)的不符合項(xiàng)中出現(xiàn)問(wèn)題最多的4個(gè)規(guī)范章節(jié)進(jìn)行梳理:
(一)設(shè)計(jì)開發(fā)
現(xiàn)場(chǎng)檢查發(fā)現(xiàn)設(shè)計(jì)過(guò)程控制存在不足�,主要體現(xiàn)在以下幾方面:(1)注冊(cè)人委托生產(chǎn)企業(yè)進(jìn)行生產(chǎn)時(shí),委托協(xié)議中雙方對(duì)研發(fā)的職責(zé)不明確���,注冊(cè)人和受托生產(chǎn)企業(yè)對(duì)設(shè)計(jì)文件的轉(zhuǎn)移不充分����。(2)設(shè)計(jì)開發(fā)研發(fā)過(guò)程和輸出資料缺失�����。如現(xiàn)場(chǎng)未查見主控板的元器件���、BOM清單、技術(shù)圖紙�、主板電路原理圖、軟件源代碼等技術(shù)研發(fā)資料���,或與實(shí)際生產(chǎn)樣機(jī)��、產(chǎn)品說(shuō)明書存在不一致�。(3)設(shè)計(jì)驗(yàn)證不充分�����。如缺少對(duì)產(chǎn)品主要性能參數(shù)或與外部配合使用器械的驗(yàn)證及相關(guān)記錄,產(chǎn)品部分功能未在技術(shù)要求中提及���,未完成相關(guān)驗(yàn)證�。(4)設(shè)計(jì)變更未進(jìn)行及時(shí)的識(shí)別�����、評(píng)審��、驗(yàn)證和確認(rèn)��。(5)產(chǎn)品風(fēng)險(xiǎn)分析及控制措施評(píng)價(jià)不充分�����,如產(chǎn)品開發(fā)新功能時(shí)未充分考慮臨床使用過(guò)程中的風(fēng)險(xiǎn)�,未考慮產(chǎn)品故障情況下的非預(yù)期使用可能產(chǎn)生的風(fēng)險(xiǎn)。
(二)采購(gòu)管理
現(xiàn)場(chǎng)檢查主要發(fā)現(xiàn)采購(gòu)質(zhì)量協(xié)議中未明確采購(gòu)要求�、主要部件未能滿足采購(gòu)追溯等問(wèn)題,主要體現(xiàn)在以下幾方面:(1)采購(gòu)質(zhì)量協(xié)議或采購(gòu)合同中對(duì)主要采購(gòu)部件的材質(zhì)�����、性能、技術(shù)參數(shù)�����、質(zhì)量標(biāo)準(zhǔn)等方面未做明確要求����。(2)原材料的進(jìn)貨檢驗(yàn)規(guī)范或驗(yàn)證內(nèi)容浮于表面,僅對(duì)外觀�、尺寸提出要求,未覆蓋關(guān)鍵性能參數(shù)���,與技術(shù)要求中整機(jī)性能參數(shù)有沖突���。(3)涉及軟件委外研發(fā)時(shí)�,開發(fā)協(xié)議中未明確軟件需求、交付技術(shù)文件內(nèi)容����、驗(yàn)收標(biāo)準(zhǔn)、軟件更新及維護(hù)等內(nèi)容����。(4)關(guān)鍵部件未能追溯到供方的批號(hào)���,對(duì)原材料批量問(wèn)題無(wú)法開展分析和追溯。
(三)生產(chǎn)控制
現(xiàn)場(chǎng)檢查發(fā)現(xiàn)生產(chǎn)工藝不充分或關(guān)鍵控制點(diǎn)不明確����、生產(chǎn)記錄不完整、主要零/部件無(wú)法追溯等問(wèn)題�����,主要體現(xiàn)在以下幾方面:(1)部分企業(yè)存在生產(chǎn)過(guò)程簡(jiǎn)單的問(wèn)題�����,未對(duì)產(chǎn)品生產(chǎn)工序進(jìn)行合理�、有效分解細(xì)化,過(guò)度依賴部件模塊化����。(2)未對(duì)調(diào)試等關(guān)鍵工序制定詳細(xì)的作業(yè)指導(dǎo)書,存在依據(jù)經(jīng)驗(yàn)進(jìn)行生產(chǎn)的情況�。(3)生產(chǎn)過(guò)程未按照作業(yè)指導(dǎo)書中的要求執(zhí)行,生產(chǎn)記錄簡(jiǎn)單�,未記錄關(guān)鍵部件序列號(hào)或編號(hào)、軟件完整版本號(hào),無(wú)法滿足可追溯的要求���。
(四)質(zhì)量管控
現(xiàn)場(chǎng)檢查發(fā)現(xiàn)檢驗(yàn)規(guī)程不充分��、檢驗(yàn)記錄不完整����、檢驗(yàn)過(guò)程無(wú)法追溯等問(wèn)題�,主要體現(xiàn)在以下幾方面:(1)對(duì)檢驗(yàn)規(guī)程未能覆蓋產(chǎn)品技術(shù)要求的檢驗(yàn)項(xiàng)目,也未采取抽檢或過(guò)程控制等有效的質(zhì)量管控方式����。(2)檢驗(yàn)方法與產(chǎn)品技術(shù)要求或國(guó)家標(biāo)準(zhǔn)有區(qū)別時(shí),企業(yè)未對(duì)所采用的方法進(jìn)行科學(xué)有效的確認(rèn)���,未能提供上述不同方法的等同性說(shuō)明��。(3)檢驗(yàn)記錄缺少原始數(shù)值記錄����,檢驗(yàn)結(jié)果無(wú)法重現(xiàn)或追溯���。(4)對(duì)于檢驗(yàn)條件和設(shè)備要求較高,企業(yè)不具備檢驗(yàn)?zāi)芰Φ模参次芯哂匈Y質(zhì)的機(jī)構(gòu)進(jìn)行檢驗(yàn)���,以證明產(chǎn)品符合強(qiáng)制性標(biāo)準(zhǔn)和經(jīng)注冊(cè)的產(chǎn)品技術(shù)要求�。(5)產(chǎn)品分別存在使用模式和檢驗(yàn)?zāi)J降那闆r下�,未對(duì)檢驗(yàn)用軟件進(jìn)行充分確認(rèn)。
如有上海市有源醫(yī)療器械注冊(cè)代辦服務(wù)需求�����,歡迎您隨時(shí)方便與杭州證標(biāo)客醫(yī)藥技術(shù)咨詢有限公司聯(lián)絡(luò)��,聯(lián)系人:葉工�,電話:18058734169,微信同��。