浙江省藥監(jiān)局公開發(fā)布的數(shù)據(jù)��,浙江省藥監(jiān)局2022年12月共收到5項創(chuàng)新醫(yī)療器械特別審查申請�,但是最終批準(zhǔn)0項。國家鼓勵醫(yī)療器械創(chuàng)新����,政府各個層級都出臺了多個創(chuàng)新醫(yī)療器械鼓勵政策,什么樣的醫(yī)療器械算是創(chuàng)新醫(yī)療器械呢���,申請申請創(chuàng)新醫(yī)療器械有什么要求�。
浙江省藥監(jiān)局公開發(fā)布的數(shù)據(jù)����,浙江省藥監(jiān)局2022年12月共收到5項創(chuàng)新醫(yī)療器械特別審查申請,但是最終批準(zhǔn)0項�����。國家鼓勵醫(yī)療器械創(chuàng)新��,政府各個層級都出臺了多個創(chuàng)新醫(yī)療器械鼓勵政策,什么樣的醫(yī)療器械算是創(chuàng)新醫(yī)療器械呢���,申請申請創(chuàng)新醫(yī)療器械有什么要求�����。

一��、2022年12月����,浙江省藥監(jiān)局批準(zhǔn)創(chuàng)新醫(yī)療器械特別審查申請0項
浙江省藥監(jiān)局發(fā)布“2022年12月審評工作情況”�,公開了2022年11月21日至12月20日注冊審評及創(chuàng)新醫(yī)療器械特別審查申請、批準(zhǔn)工作情況���,其中�����,浙江省藥監(jiān)局12月批準(zhǔn)創(chuàng)新醫(yī)療器械特別審查申請0項,如下圖所示:
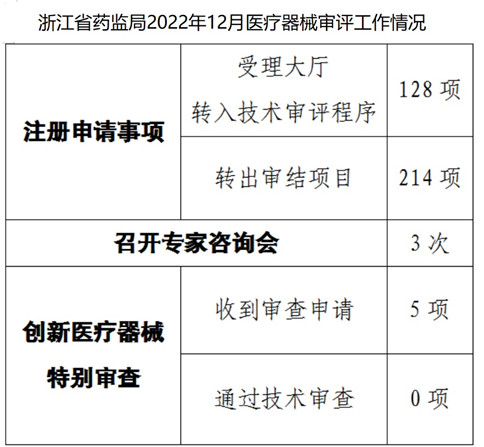
從以上創(chuàng)新醫(yī)療器械申請及批準(zhǔn)情況�����,大家也能看到創(chuàng)新醫(yī)療器械特別審查及其審批必須符合一定的條件和要求。
二�、浙江省申請創(chuàng)新醫(yī)療器械有什么要求?
1.申請人經(jīng)過其技術(shù)創(chuàng)新活動��,在中國依法擁有產(chǎn)品核心技術(shù)發(fā)明專利權(quán)���,或者依法通過受讓取得在中國發(fā)明專利權(quán)或其使用權(quán)�����;或者核心技術(shù)發(fā)明專利的申請已由國務(wù)院專利行政部門公開��。
2.產(chǎn)品主要工作原理/作用機理為國內(nèi)首創(chuàng)���,產(chǎn)品性能或者安全性與同類產(chǎn)品比較有根本性改進,技術(shù)上處于國際領(lǐng)先水平�,并且具有顯著的臨床應(yīng)用價值。
3.申請人已完成產(chǎn)品的前期研究并具有基本定型產(chǎn)品�����,研究過程真實和受控�,研究數(shù)據(jù)完整和可溯源。
以上3條要求是浙江省申請創(chuàng)新醫(yī)療器械的基本要求�。