歐盟的Basic UDI-DI是歐盟醫(yī)療器械CE認(rèn)證?法規(guī)中的一個(gè)概念�����,是器械類型的主要識(shí)別符���,該代碼與UDI-DI不同。UDI-DI跟著產(chǎn)品走�����,體現(xiàn)在產(chǎn)品、包裝和標(biāo)簽上�����,實(shí)現(xiàn)的是產(chǎn)品追溯目的�����;而Basic UDI-DI跟著文件走����,體現(xiàn)在證書、符合性聲明和技術(shù)文件中����,實(shí)現(xiàn)的是文件對(duì)應(yīng)的產(chǎn)品組的識(shí)別。
歐盟的Basic UDI-DI是歐盟醫(yī)療器械CE認(rèn)證法規(guī)中的一個(gè)概念��,是器械類型的主要識(shí)別符�,該代碼與UDI-DI不同。UDI-DI跟著產(chǎn)品走���,體現(xiàn)在產(chǎn)品���、包裝和標(biāo)簽上�,實(shí)現(xiàn)的是產(chǎn)品追溯目的����;而Basic UDI-DI跟著文件走,體現(xiàn)在證書�����、符合性聲明和技術(shù)文件中����,實(shí)現(xiàn)的是文件對(duì)應(yīng)的產(chǎn)品組的識(shí)別。Basic UDI-DI的要求已經(jīng)于2021年5月26日開始生效���,廣大制造商需要盡快申請(qǐng)編碼并納入自身的MDR文件體系�����。
一�����、Basic UDI-DI和UDI-DI的差別
Basic UDI-DI是在醫(yī)療器械的一個(gè)器械組層面上分配DI并完成賦碼,這個(gè)和原來UDI-DI需要針對(duì)每一組別產(chǎn)品中的每個(gè)規(guī)格,每個(gè)包裝規(guī)格分別賦碼是不同的���。如下圖:5毫升和10毫升的注射器��,分別按照100支裝箱�����;那么UDI-DI就會(huì)有4個(gè)DI號(hào)碼�����,而此時(shí)對(duì)應(yīng)的Basic UDI-DI只有一個(gè)統(tǒng)一編碼���。

二、Basic UDI-DI的用處
Basic UDI-DI是EUDAMED數(shù)據(jù)庫中關(guān)鍵信息����,同時(shí)會(huì)體現(xiàn)在CE證書、歐盟符合性聲明和技術(shù)文件中�����。

三��、Basic UDI-DI的結(jié)構(gòu)
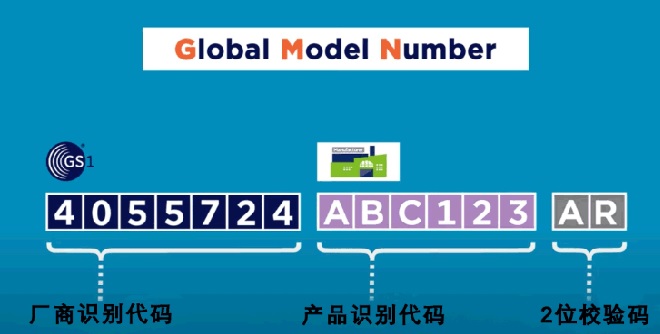
Basic UDI-DI是由Company Prefix + Model Reference+校驗(yàn)碼組成,長(zhǎng)度不能超過25位��。其中�,Company Prefix即廠商識(shí)別代碼,與UDI中的一致�����。Model Reference�����,也就是產(chǎn)品識(shí)別代碼��,是由企業(yè)自行編制的��,可以是字母+數(shù)字的形式�。
四、Basic UDI-DI的生成
確定了廠商識(shí)別碼和器械識(shí)別碼之后��,還需要生成校驗(yàn)碼�����。校驗(yàn)碼可以使用GS1網(wǎng)站的工具生成��。
如下圖��,輸入廠商識(shí)別碼69712345和器械識(shí)別碼SYR001之后����,校驗(yàn)碼V6會(huì)自動(dòng)生成。

任何疑問�����,歡迎您隨時(shí)方便與杭州證標(biāo)客聯(lián)系����。